Hoà tan hết 12g một kim loại ( hoá trị II) bằng dung dịch H 2 S O 4 loãng thu được 6,72 lít khí H 2 (đktc). Kim loại này là
A. Zn
B. Fe
C. Ca
D. Mg
Hoà tan hết 12g một kim loại ( hoá trị II) bằng dung dịch H 2 S O 4 loãng thu được 6,72 lít khí H 2 (đktc). Kim loại này là
A. Zn
B. Fe
C. Ca
D. Mg
Hoà tan hết 3,6g một kim loại hoá trị II bằng dung dịch H2SO4 loãng được 3,36lít H2 (đktc). Kim loại là
1.Ca.
2.Mg.
3.Zn.
4.Fe.
Gọi kim loại là M
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(PTHH:M+H_2SO_4--->MSO_4+H_2\)
Theo PT: \(n_M=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{3,6}{0,15}=24\left(g\right)\)
Vậy M là magie (Mg)
Chọn 2
Hoà tan hết 3,6 g một kim loại hoá trị II bằng dung dịch H 2 S O 4 loãng được 3,36 lít H 2 (đktc). Kim loại là
A. Zn
B. Mg
C. Fe
D. Ca
Hoà tan hết một kim loại Zn bằng dung dịch H2SO4 loãng thu được 4,958 lít khí H2 (đktc). Khối lượng Kim loại Zn cần dùng là:
A.13
B.14
C.15
D.16
Hoà tan 16,8g kim loại hoá trị II vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H 2 (đktc). Kim loại đem hoà tan là:
A. Mg
B. Zn
C. Pb
D. Fe
Hòa tan 7,2 gam kim loại hóa trị II bằng dung dịch H2SO4 loãng dư thu được 6,72 lít khí H2 (đktc).
Tìm kim loại
PTHH: \(R+H_2SO_4\rightarrow RSO_4+H_2\)
Theo PTHH: \(n_R=n_{H_2}\)
\(\Rightarrow\dfrac{7,2}{R}=\dfrac{6,72}{22,4}\) \(\Rightarrow R=24\)
Vậy kim loại cần tìm là Magie
Gọi kim loại là M
PTHH: M + H2SO4 ---> MSO4 + H2
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_M=n_{H_2}=0,3\left(mol\right)\)
=> \(M_M=\dfrac{7,2}{0,3}=24\left(g\right)\)
Dựa vào bảng hóa trị, suy ra:
M là magie (Mg)
Hoà tan hỗn hợp gồm 0,5 gam Fe và một kim loại hoá trị II trong dung dịch HCl dư thu được 1,12 lít khí H2 (đktc). Kim loại hoá trị II đó là:
A. Mg
B. Ca
C. Zn
D. Be.
Hoà tan 16,8g kim loại vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H 2 (đktc). Kim loại đem hoà tan là (Biết trong muối thu được sau phản ứng kim loại có hóa trị II)
A. Mg
B. Zn
C. Pb
D. Fe
Hoà tan hoàn toàn 0,8125g một kim loại hoá trị II và dung dịch H 2 S O 4 đặc, nóng thu được 0,28 lít khí S O 2 (đktc).Kim loại đã dùng là
A. Mg.
B. Cu.
C. Zn.
D. Fe.
Hòa tan hoàn toàn 0,5 gam Fe và một kim loại hóa trị II trong dung dịch HCl thu được 1,12 lít khí H2 đktc. Kim loại hóa trị II đó là kim loại nào sau đây.
A. Mg.
B. Ca.
C. Zn.
D. Be.
Đáp án D.
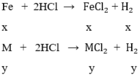
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 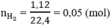
theo bài ra ta có hệ phương trình
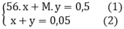
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 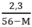
Ta có 0 < y < 0,05
y > 0 ↔ 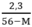 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 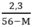 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be